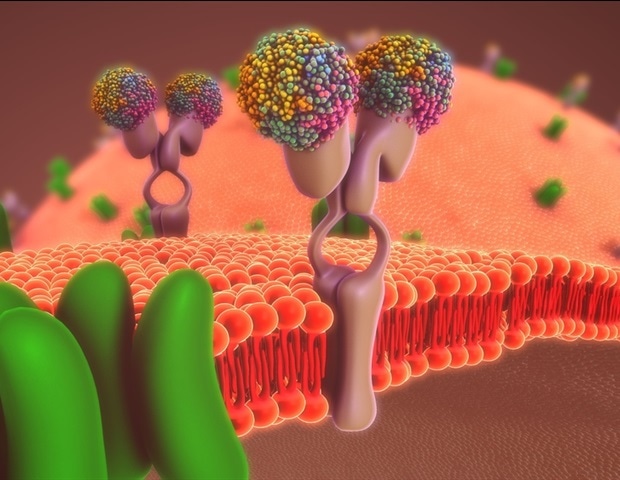
آیا تا به حال فکر کرده اید که چگونه داروها به اهداف خود می رسند و عملکرد خود را در بدن ما انجام می دهند؟ اگر یک مولکول دارو یا یک لیگاند یک پیام باشد، صندوق ورودی معمولاً یک گیرنده در غشای سلولی است. یکی از این گیرندهها که در انتقال سیگنالهای مولکولی نقش دارد، گیرنده جفتشده با پروتئین G (GPCR) است. حدود یک سوم داروهای موجود با کنترل فعال شدن این پروتئین کار می کنند. محققان ژاپنی اکنون روش جدیدی را برای فعال کردن GPCR با ایجاد تغییرات شکل در ناحیه داخل سلولی گیرنده نشان می دهند. این فرآیند جدید می تواند به محققان در طراحی داروهایی با عوارض جانبی کمتر یا بدون عوارض کمک کند.
اگر غشای سلولی مانند یک ساندویچ کوکی Oreo باشد، GPCR مانند یک مار است که هفت قسمت آن در داخل و خارج از سطح ساندویچ کوکی حرکت می کند. حلقه های خارج سلولی صندوق ورودی پیام ها هستند. هنگامی که یک مولکول پیام به سمت خارج سلولی گیرنده متصل می شود، باعث تغییر شکل می شود که پروتئین های G و پروتئین ß-arrestin متصل به سمت داخل سلولی گیرنده را فعال می کند. مانند یک رله مولکولی، اطلاعات از پایین دست عبور می کند و بر فرآیندهای مختلف بدن تأثیر می گذارد. این گونه است که ما می بینیم، بو می کنیم و می چشیم، که حسی از نور، بویایی و پیام های چشایی است.
اگر داروهایی که بر روی GPCR ها اثر می گذارند، مسیرهای سیگنال دهی متعدد را به جای یک مسیر هدف خاص فعال کنند، عوارض جانبی نامطلوب ایجاد می کنند. به همین دلیل است که توسعه دارو بر فعال کردن مسیرهای سیگنال مولکولی خاص در سلول ها متمرکز است. فعال کردن GPCR از داخل سلول به جای خارج از سلول می تواند یکی از راه های دستیابی به ویژگی باشد. اما تاکنون هیچ مدرکی مبنی بر فعال شدن مستقیم تنها سمت داخل سلولی GPCR ها بدون شروع از سمت خارج سلولی وجود نداشت.
تیمی از محققان به سرپرستی اسامو نورکی، استاد دانشگاه توکیو و آزمایشگاه او، یک حالت فعالسازی گیرنده جدید GPCR مرتبط با متابولیسم استخوان به نام گیرنده هورمون پاراتیروئید نوع 1 انسانی (PTH1R) را بدون انتقال سیگنال از خارج سلولی کشف کردند. سمت.
درک مکانیسم مولکولی ما را قادر می سازد تا داروهای بهینه را طراحی کنیم. چنین دارویی “یک درمان امیدوارکننده برای پوکی استخوان” ارائه می دهد.
کازوهیرو کوبایاشی، دانشجوی دکترا و نویسنده مطالعه
کوبایاشی از زمانی که در مقطع کارشناسی تحصیل کرده بود، در مورد تشکیل استخوان در مدل های حیوانی تحقیق می کرد. او میگوید: «درمانهای پوکی استخوان که PTH1R را هدف قرار میدهند، نیاز به دوز دقیق دارند، محدودیتهای اداری دارند و هنوز هیچ جایگزین بهتری وجود ندارد.» این موضوع باعث شد تا تیم آنها به دنبال استراتژی های طراحی بهتر دارو با هدف قرار دادن گیرنده هورمون پاراتیروئید باشند.
برای درک عملکرد از طریق ساختار، آنها از میکروسکوپ کرایو الکترونی استفاده کردند و ساختار سه بعدی پروتئین PTH1R و G متصل به یک مولکول پیام را نشان دادند. این تیم یک مولکول پیام غیر پپتیدی به نام PCO371 را سنتز کردند که به ناحیه داخل سلولی گیرنده متصل می شود و مستقیماً با زیر واحدهای پروتئین G تعامل دارد. به عبارت دیگر PCO371 پس از ورود به سلول گیرنده را فعال می کند.
ساختار PTH1R متصل به PCO371 می تواند به طور مستقیم و پایدار سمت داخل سلولی PTH1R را تعدیل کند. و از آنجا که PCO371 فقط پروتئین G را فعال می کند و نه ß-arrestin، عوارض جانبی ایجاد نمی کند. این ویژگی حالت اتصال و فعالسازی گیرنده آن را به یک کاندید مناسب برای داروهای بالقوه مبتنی بر مولکولهای کوچک برای GPCRهای کلاس B1، مانند PTH1R، که در حال حاضر فاقد لیگاندهای دارویی خوراکی هستند، تبدیل میکند. چنین داروهایی می توانند اثرات نامطلوب و بار بر روی بیماران را کاهش دهند زیرا آنها در مسیرهای مولکولی خاص عمل می کنند.
یافته های این مطالعه به “توسعه داروهای جدید برای اختلالاتی مانند چاقی، درد، پوکی استخوان و اختلالات عصبی کمک می کند.”
این مطالعه در مجله ظاهر می شود طبیعت.
منبع:
مرجع مجله:
کوبایاشی، ک. و همکاران. (2023). فعال سازی GPCR کلاس B1 توسط آگونیست داخل سلولی. طبیعت. doi.org/10.1038/s41586-023-06169-3.

